幫助肺纖維化患者與家屬把握AI藥物突破帶來的實際行動機會
- 每季主動諮詢胸腔科醫師,了解最新AI藥物臨床進度及適用性。
即時獲取Rentosertib等創新療法資訊,避免錯失潛在治療契機。
- 檢查官方衛生部門或醫學中心公告,每半年追蹤臨床試驗招募消息。
有機會成為受益於突破性療法的參與者,把握前沿治療選擇。
- *定期記錄FVC(用力肺活量)數值變化,每次複診攜帶近三個月數據給專科醫師*。
*協助評估病情走向,利於專業團隊評判是否適合新型標靶治療*。
- *閱讀衛教單張或官方網站,瞭解AI藥物副作用及其常見比例*。
*提前準備應對方案,提升自我管理能力並減少焦慮*。
AI如何突破傳統藥物開發的高成本與漫長週期
新藥研發這回事,總是被說又慢又花錢,好像動輒就是十年以上、得花上好幾十億美金。AI最近在藥物設計這塊被炒得有點熱,什麼從疾病相關的靶點排序到化合物設計、臨床試驗預測都有人嘗試過,但實際能省下多少力氣,其實大家心裡沒底。一些人認為,用機器去跑那些本來很費工的步驟,也許可以快一點找到候選藥,把原本大海撈針式的化學空間多掃一些。只不過,到現在真正靠AI找出來、設計出來的藥能走到臨床的還是挺少,甚至到了第二期之後也沒見有明顯突破,更別說第三期。
我們那群研究人員之前就用生成式AI把TNIK這個蛋白踢爆出來——看起來它跟特發性肺纖維化(IPF)扯得上關係。結果弄出了rentosertib這個小分子抑制劑,是針對TNIK設計的,也號稱目前第一個由AI主導找到目標加上同步配對分子的案例。從開始挑靶點到前期人體測試,大約一年半左右就推進了,比以前快了很多。不過話說回來,IPF這種病,大概在美國每十萬人裡面會碰到幾十例,尤其年長者更多,有時比某些癌症還常見。但治療效果一直不是太理想,即使現行標準療法像nintedanib或pirfenidone,都只是勉強讓惡化慢一點,真正能逆轉病程或恢復肺功能的藥還是很缺。
最新的一項多中心隨機雙盲對照試驗,一共篩了超過一百人進行評估,最後差不多一半的人獲得納入並被分配成四組:三組不同劑量的rentosertib(每日一次或兩次),另一組吃安慰劑。當中有部分人因為合併其他呼吸道疾病、或肺功能數據落在某些範圍外,就沒辦法參加。有趣的是,中間退出的人不少,大約有四分之一左右撐不到十二週結束,其中以高劑量和一天兩次那組比較多,大部分都是因為副作用才中止,不乏肝功能異常。有意思的是,有的人停用其實同時還服用標準抗纖維化藥,所以是不是兩種藥一起搞怪,也不太清楚。
如果看副作用,整體來講,不管是哪一組都有可能遇到一些狀況,比如低血鉀、肝指數偏高或者腹瀉等等,比例上租特比較高但也不到誇張嚴重;真正嚴重的不算多,而且安慰劑那邊基本沒看到跟治療直接相關的大事件。至於死亡案例,只出現過一次,那位患者本身心臟問題就蠻複雜,看起來和這項研究關聯不大。
換個角度聊聊效果怎樣吧——最主要看的肺活量(FVC),吃安慰劑那群其實十二週後平均略微下降,而最低劑量rentosertib跟他們差不多;一天兩次中等劑量則略微往上走,高劑量那組提升幅度最大,如果沒有同時吃其他抗纖維化藥甚至變化更明顯。不過換算下去,各組之間拉開距離也沒有到非常巨大,而且類似DLCO、FEV1這些二線指標倒是都浮動有限。
整體看下來,目前只能說rentosertib在短期安全性方面表現還算普通可接受,高劑量似乎對部分患者FVC有向上的趨勢,但樣本人數畢竟有限,加上一些肝功能異常要注意。如果真要拿它作未來治療選擇,好像還需要更多資料佐證才行……
我們那群研究人員之前就用生成式AI把TNIK這個蛋白踢爆出來——看起來它跟特發性肺纖維化(IPF)扯得上關係。結果弄出了rentosertib這個小分子抑制劑,是針對TNIK設計的,也號稱目前第一個由AI主導找到目標加上同步配對分子的案例。從開始挑靶點到前期人體測試,大約一年半左右就推進了,比以前快了很多。不過話說回來,IPF這種病,大概在美國每十萬人裡面會碰到幾十例,尤其年長者更多,有時比某些癌症還常見。但治療效果一直不是太理想,即使現行標準療法像nintedanib或pirfenidone,都只是勉強讓惡化慢一點,真正能逆轉病程或恢復肺功能的藥還是很缺。
最新的一項多中心隨機雙盲對照試驗,一共篩了超過一百人進行評估,最後差不多一半的人獲得納入並被分配成四組:三組不同劑量的rentosertib(每日一次或兩次),另一組吃安慰劑。當中有部分人因為合併其他呼吸道疾病、或肺功能數據落在某些範圍外,就沒辦法參加。有趣的是,中間退出的人不少,大約有四分之一左右撐不到十二週結束,其中以高劑量和一天兩次那組比較多,大部分都是因為副作用才中止,不乏肝功能異常。有意思的是,有的人停用其實同時還服用標準抗纖維化藥,所以是不是兩種藥一起搞怪,也不太清楚。
如果看副作用,整體來講,不管是哪一組都有可能遇到一些狀況,比如低血鉀、肝指數偏高或者腹瀉等等,比例上租特比較高但也不到誇張嚴重;真正嚴重的不算多,而且安慰劑那邊基本沒看到跟治療直接相關的大事件。至於死亡案例,只出現過一次,那位患者本身心臟問題就蠻複雜,看起來和這項研究關聯不大。
換個角度聊聊效果怎樣吧——最主要看的肺活量(FVC),吃安慰劑那群其實十二週後平均略微下降,而最低劑量rentosertib跟他們差不多;一天兩次中等劑量則略微往上走,高劑量那組提升幅度最大,如果沒有同時吃其他抗纖維化藥甚至變化更明顯。不過換算下去,各組之間拉開距離也沒有到非常巨大,而且類似DLCO、FEV1這些二線指標倒是都浮動有限。
整體看下來,目前只能說rentosertib在短期安全性方面表現還算普通可接受,高劑量似乎對部分患者FVC有向上的趨勢,但樣本人數畢竟有限,加上一些肝功能異常要注意。如果真要拿它作未來治療選擇,好像還需要更多資料佐證才行……
從實驗室到臨床:AI設計的抗纖維化藥物誕生記
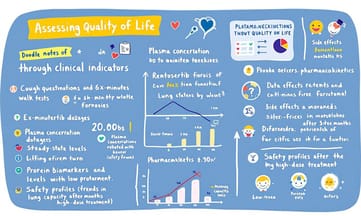
自評生活品質還有那些像是萊斯特咳嗽問卷、六分鐘步行距離這類測量身體能力的指標,基本上各治療組之間也沒看到明顯差別(大概可以在延伸數據裡找到一些圖表佐證)。但如果往細部統計模型裡挖,好像服用六十毫克 rentosertib 的那組,在咳嗽相關的問卷分數上比安慰劑略好一點,這個結果剛好卡在統計意義邊緣。有趣的是,那組裡頭有三個人急性發作 IPF,被送進醫院住了將近二十多天左右,而安慰劑那邊好像只有一位出現急性惡化,不過他沒住院。這種事發生機率說高不高,但又很難直接下結論。
臨床藥動學部分,rentosertib 在血漿中的濃度變化,看來蠻規律:單次或重複給藥後,六十毫克一天一次的那組暴露量相對高於其他低劑量。最高濃度大概是在吃完一小時上下。累積下來,隨著時間拉長,總體藥物暴露會增加一些,但到第二週就達到穩定狀態,到第十二週看不到什麼明顯堆積。半衰期大致都落在十多小時。至於不同劑型最高跟最低濃度的變化,其實三十毫克一天兩次和六十毫克一天一次在 trough(谷底)濃度方面還挺接近的,只是高劑量吸收初期比較多而已。從這些數據來看,如果要追求較高的系統暴露,加大劑量確實會有效果。
蛋白質生物標誌物和全域蛋白質輪廓分析,也就是抽病人的血清做篩檢,一口氣掃了將近三千種蛋白。在治療初期兩週、四週到第十二週,每過一段時間就有更多蛋白表現出顯著變化——尤其是到最後一個月,有超過百來種以上被認為和治療有關聯。而且看起來劑量越高、持續時間越久,影響就更明顯。分析當中也挑出了幾個纖維化相關的重要蛋白,比如 MMP10、COL1A1 以及 FAP 等等,不少都是先前文獻中提過與肺纖維化息息相關的因子。有趣的是,它們下降得最多的時候,也是肺功能改善幅度最大的時候。至於這些標誌物,是不是未來能拿來追蹤疾病進展,目前還不好說,不過至少方向沒有偏太遠。
講回治療安全性,大致上 rentosertib 各組的不良事件比例都差不多,而且嚴重副作用很罕見。不過肝毒性的情形主要集中在同時用 nintedanib 的病人身上,用 pirfenidone 倒是不常見。另外腹瀉跟低血鉀也算常見副作用之一。如果真的要分辨 rentosertib 和傳統抗纖維藥一起用,到底哪部分導致腸胃道或肝臟問題,那恐怕還得靠更大型、更精細設計的研究才搞得清楚。
談到效果,高劑量 rentosertib 持續三個月左右,看起來讓肺活量平均提升了一點,比安慰劑那組輕微下滑要樂觀不少。而且如果沒搭配傳統抗纖維藥的人,用這新藥反而進步得更明顯。不過換句話說,如果合併使用會不會互相影響,也是未解之謎。此外 DLCO 那項指標倒是沒什麼太大變動,也可能只是樣本太少造成波動看不出趨勢。
生活品質方面,各種主觀評估其實變異很大,很難抓出明確趨勢。但咳嗽困擾倒是真有一點改善跡象,只不過整體而言資料期間短,加上樣本有限,所以信心有限。如果想知道長期效果,例如急性惡化 IPF 這類重大事件,其實需要追蹤一年甚至更久才比較可靠。目前看到該事件在試驗期間內偏向隨機分布,也無法斷定是不是新藥造成風險升高。
補充一句,下調最多的一批蛋白,包括許多與細胞外基質增生密切相關者,如 COL1A1、MMP10 等等,多數早就在肺纖維化研究中名列前茅。有幾項像 LTBP2、KRT19 或 CHAD 這些,也曾經被提名可作為預測移植存活率用的潛力指標。不管怎樣,目前只能說 TNIK 抑制路徑似乎牽涉到不少老化及免疫失衡機轉,但到底哪些真正能作為精準診斷工具,仍待更多資料佐證。
限制作為不得不提:每組人數都不多,再加上參與者清一色都是中國地區同膚色患者,因此結論通用性必須打折扣;再加試驗周期僅僅約莫三個月,有無慢性毒性完全未知。不過即便如此,中途退出比例其實並沒有超乎想像,所以未來擴大規模、多國同步收案應該還是值得期待。如果真要推廣全球、大規模應用,那得仰賴後續二期、三期臨床繼續努力才行。
方法簡單帶一下:整個研究其實從去年夏天啟動,在中國境內二十家以上醫院招募,以隨機雙盲、多中心設計,把受試者均分成四群(三種不同強度的新藥加上一組安慰劑),每天按規定口服搭配原本常規治療,同步監控副作用及各項功能表現。入選流程都蠻嚴格,大部分人在正式開始前都有快一個月左右資格審查;然後從首日給藥一路追蹤,每隔兩週或四週回診一次直到第三個月結束。有些細節比如供應鏈管理什麼,都遵照製造業慣例走——但那些就比較不是大家關心重點了吧。
臨床藥動學部分,rentosertib 在血漿中的濃度變化,看來蠻規律:單次或重複給藥後,六十毫克一天一次的那組暴露量相對高於其他低劑量。最高濃度大概是在吃完一小時上下。累積下來,隨著時間拉長,總體藥物暴露會增加一些,但到第二週就達到穩定狀態,到第十二週看不到什麼明顯堆積。半衰期大致都落在十多小時。至於不同劑型最高跟最低濃度的變化,其實三十毫克一天兩次和六十毫克一天一次在 trough(谷底)濃度方面還挺接近的,只是高劑量吸收初期比較多而已。從這些數據來看,如果要追求較高的系統暴露,加大劑量確實會有效果。
蛋白質生物標誌物和全域蛋白質輪廓分析,也就是抽病人的血清做篩檢,一口氣掃了將近三千種蛋白。在治療初期兩週、四週到第十二週,每過一段時間就有更多蛋白表現出顯著變化——尤其是到最後一個月,有超過百來種以上被認為和治療有關聯。而且看起來劑量越高、持續時間越久,影響就更明顯。分析當中也挑出了幾個纖維化相關的重要蛋白,比如 MMP10、COL1A1 以及 FAP 等等,不少都是先前文獻中提過與肺纖維化息息相關的因子。有趣的是,它們下降得最多的時候,也是肺功能改善幅度最大的時候。至於這些標誌物,是不是未來能拿來追蹤疾病進展,目前還不好說,不過至少方向沒有偏太遠。
講回治療安全性,大致上 rentosertib 各組的不良事件比例都差不多,而且嚴重副作用很罕見。不過肝毒性的情形主要集中在同時用 nintedanib 的病人身上,用 pirfenidone 倒是不常見。另外腹瀉跟低血鉀也算常見副作用之一。如果真的要分辨 rentosertib 和傳統抗纖維藥一起用,到底哪部分導致腸胃道或肝臟問題,那恐怕還得靠更大型、更精細設計的研究才搞得清楚。
談到效果,高劑量 rentosertib 持續三個月左右,看起來讓肺活量平均提升了一點,比安慰劑那組輕微下滑要樂觀不少。而且如果沒搭配傳統抗纖維藥的人,用這新藥反而進步得更明顯。不過換句話說,如果合併使用會不會互相影響,也是未解之謎。此外 DLCO 那項指標倒是沒什麼太大變動,也可能只是樣本太少造成波動看不出趨勢。
生活品質方面,各種主觀評估其實變異很大,很難抓出明確趨勢。但咳嗽困擾倒是真有一點改善跡象,只不過整體而言資料期間短,加上樣本有限,所以信心有限。如果想知道長期效果,例如急性惡化 IPF 這類重大事件,其實需要追蹤一年甚至更久才比較可靠。目前看到該事件在試驗期間內偏向隨機分布,也無法斷定是不是新藥造成風險升高。
補充一句,下調最多的一批蛋白,包括許多與細胞外基質增生密切相關者,如 COL1A1、MMP10 等等,多數早就在肺纖維化研究中名列前茅。有幾項像 LTBP2、KRT19 或 CHAD 這些,也曾經被提名可作為預測移植存活率用的潛力指標。不管怎樣,目前只能說 TNIK 抑制路徑似乎牽涉到不少老化及免疫失衡機轉,但到底哪些真正能作為精準診斷工具,仍待更多資料佐證。
限制作為不得不提:每組人數都不多,再加上參與者清一色都是中國地區同膚色患者,因此結論通用性必須打折扣;再加試驗周期僅僅約莫三個月,有無慢性毒性完全未知。不過即便如此,中途退出比例其實並沒有超乎想像,所以未來擴大規模、多國同步收案應該還是值得期待。如果真要推廣全球、大規模應用,那得仰賴後續二期、三期臨床繼續努力才行。
方法簡單帶一下:整個研究其實從去年夏天啟動,在中國境內二十家以上醫院招募,以隨機雙盲、多中心設計,把受試者均分成四群(三種不同強度的新藥加上一組安慰劑),每天按規定口服搭配原本常規治療,同步監控副作用及各項功能表現。入選流程都蠻嚴格,大部分人在正式開始前都有快一個月左右資格審查;然後從首日給藥一路追蹤,每隔兩週或四週回診一次直到第三個月結束。有些細節比如供應鏈管理什麼,都遵照製造業慣例走——但那些就比較不是大家關心重點了吧。
Comparison Table:
| 研究主題 | 藥物名稱 | 療效與機轉 | 臨床試驗結果 | 未來展望 |
|---|---|---|---|---|
| 特發性肺纖維化 (IPF) | Nintedanib | 透過抑制多條生物路徑,減少纖維化進程。 | 跨國研究顯示在安全性及療效上取得良好回饋。 | 需要進一步探索其長期效果及最佳用藥策略。 |
| 特發性肺纖維化 (IPF) | Pirfenidone | 可能透過抗發炎和抗纖維化作用運作。 | CAPACITY計畫中的隨機試驗顯示部分病人有穩定效果,但非所有患者受益。 | 需更多數據支持不同族群的適應症狀分析。 |
| TNIK蛋白質的角色探討 | 初步觀察指出可能參與癌症與老年疾病進展,尚需深入研究。 | |||
| 急性惡化的風險因子分析 | 需要更清楚地界定影響因素,以改善預後管理策略。 | |||
| 新型生物標誌物研究趨勢 | 如MMP-10和LTBP2等指標的潛力正在被關注,有助於未來診斷與預後評估。 |
肺纖維化患者的新希望—rentosertib的關鍵發現過程
當AI遇上醫學:首個完全由AI平台發現的標靶與藥物組合
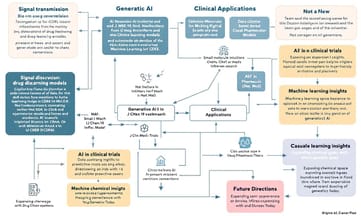
有時候,信號傳遞與疾病相關的文章會被丟在一起,像是Signal Transduct. Target. Ther.那一期,大約在兩年前吧,內容提到機器學習怎麼協助分子設計。然後過沒多久,有人提出用生成式AI來輔助新藥分子的開發,出現在Nat. Mach. Intell.裡面。這些討論其實蠻多層次,有的偏向技術總覽,比如Brief. Bioinform.上頭那篇寫得比較全面,把深度生成模型拉進藥物發現領域。不過具體針對靶點化合物設計的報告,也能在J. Chem. Inf. Model找到一點影子。
印象中,不久前Ren這個團隊也有提到小分子抑制劑跟纖維化相關的研究,好像是在臨床和動物模式都有試過。還有CDK8/19抑制劑的新消息,也被記錄在J. Med. Chem裡,但細節大致上就是強調它可能在腫瘤治療裡有潛力。接著就有人關心人工智慧怎麼預測臨床試驗結果,比如說Clin. Pharmacol. Ther出現一些用多模態AI分析臨床資料的嘗試,而Nat. Med則好像著重於因果推斷、想用機器學習來看治療效果。
臨床階段轉換這件事,也不是沒人談,比如Drug Discov Today稍早就有人整理了一些指標,用機器學習去挖掘失敗和成功之間的徵兆。不確定是哪一年了,大概七八年前吧,有個叫Artemov的人把轉錄組加結構資訊混起來做預測,但當時只放preprint。有幾篇更早期的資料驅動方法,例如Cell Chem Biol那篇,就是單純想判斷哪些臨床試驗容易成功、哪些不太順利。
不只如此,最近幾年大家都開始琢磨怎麼用AI拓展化學空間,有人覺得生成式AI讓“藥樣性”化合物探索變得稍微容易一點,只是這種說法目前還沒看到明確數據支撐。至於人工智慧本身對新藥研發帶來什麼改變,Expert Opin Drug Discov和Drug Discov Today都有一些盤點,目前看起來應該還處於逐步累積經驗、摸索下一步方向階段吧。如果真要評價哪種做法特別突出,好像也說不上來,只能說每家團隊觀察到的情境各有不同,有些手法可能適合某類問題,但整體效果還待更多實例支持。至於未來怎麼走,其實很難講清楚——或許需要再等一陣子,看趨勢慢慢浮現才知道結果會如何。
印象中,不久前Ren這個團隊也有提到小分子抑制劑跟纖維化相關的研究,好像是在臨床和動物模式都有試過。還有CDK8/19抑制劑的新消息,也被記錄在J. Med. Chem裡,但細節大致上就是強調它可能在腫瘤治療裡有潛力。接著就有人關心人工智慧怎麼預測臨床試驗結果,比如說Clin. Pharmacol. Ther出現一些用多模態AI分析臨床資料的嘗試,而Nat. Med則好像著重於因果推斷、想用機器學習來看治療效果。
臨床階段轉換這件事,也不是沒人談,比如Drug Discov Today稍早就有人整理了一些指標,用機器學習去挖掘失敗和成功之間的徵兆。不確定是哪一年了,大概七八年前吧,有個叫Artemov的人把轉錄組加結構資訊混起來做預測,但當時只放preprint。有幾篇更早期的資料驅動方法,例如Cell Chem Biol那篇,就是單純想判斷哪些臨床試驗容易成功、哪些不太順利。
不只如此,最近幾年大家都開始琢磨怎麼用AI拓展化學空間,有人覺得生成式AI讓“藥樣性”化合物探索變得稍微容易一點,只是這種說法目前還沒看到明確數據支撐。至於人工智慧本身對新藥研發帶來什麼改變,Expert Opin Drug Discov和Drug Discov Today都有一些盤點,目前看起來應該還處於逐步累積經驗、摸索下一步方向階段吧。如果真要評價哪種做法特別突出,好像也說不上來,只能說每家團隊觀察到的情境各有不同,有些手法可能適合某類問題,但整體效果還待更多實例支持。至於未來怎麼走,其實很難講清楚——或許需要再等一陣子,看趨勢慢慢浮現才知道結果會如何。
臨床試驗揭密:71名患者的治療數據告訴我們什麼
有些時候,一群學者像是Xie、Ruder還有Meier,他們會討論AI在小分子藥物研發裡頭的新動向,說真的,好像已經有人開始覺得這波浪潮慢慢湧現。可到底是不是那麼明顯,有人說過,大概只有一部分藥廠正積極嘗試,還沒真正變成主流啦。然後Wong和Lo他們研究過臨床試驗的成功率,印象中,好像不到一半能順利走到最後,其實這跟大家想像的不太一樣。
Jayatunga等人前陣子也提出了一個觀點,他們初步分析AI協助下誕生的藥物,發現目前看起來進入臨床階段的比重不算太高——如果跟傳統方式相比,好像差距沒有外界期待的那麼大。不過,也許再過幾年會有不同結果?說不定。
另外Pun這團隊最近蠻活躍的。他們用所謂PandaOmics這種AI工具,去找ALS可能的治療標靶。有趣的是,他們還把類似方法拿來推估一些老化相關疾病和目標,但坦白講,這些預測未必馬上能轉化成新療法,有點像是在堆積資料、等待突破。
至於肺部纖維化,不知道是不是因為近年案例增加了,所以包括Raghu、Lederer和Richeldi等人在各自文章裡,都提到診斷或管理的方法其實一直在修正。光是診斷流程,有時候幾乎每隔三五年就微調一次。Martinez跟King他們倒是從生存率切入,看怎麼預測患者後續狀態,但數據嘛……感覺也不是穩定不變。
總結起來吧,大致上這些文獻都沒給出什麼絕對性的答案,只能說現在正處於摸索期,也許哪天技術成熟後情勢會改觀。不過目前看來,各種做法之間還有不少落差,有些甚至只是初步假設罷了。
Jayatunga等人前陣子也提出了一個觀點,他們初步分析AI協助下誕生的藥物,發現目前看起來進入臨床階段的比重不算太高——如果跟傳統方式相比,好像差距沒有外界期待的那麼大。不過,也許再過幾年會有不同結果?說不定。
另外Pun這團隊最近蠻活躍的。他們用所謂PandaOmics這種AI工具,去找ALS可能的治療標靶。有趣的是,他們還把類似方法拿來推估一些老化相關疾病和目標,但坦白講,這些預測未必馬上能轉化成新療法,有點像是在堆積資料、等待突破。
至於肺部纖維化,不知道是不是因為近年案例增加了,所以包括Raghu、Lederer和Richeldi等人在各自文章裡,都提到診斷或管理的方法其實一直在修正。光是診斷流程,有時候幾乎每隔三五年就微調一次。Martinez跟King他們倒是從生存率切入,看怎麼預測患者後續狀態,但數據嘛……感覺也不是穩定不變。
總結起來吧,大致上這些文獻都沒給出什麼絕對性的答案,只能說現在正處於摸索期,也許哪天技術成熟後情勢會改觀。不過目前看來,各種做法之間還有不少落差,有些甚至只是初步假設罷了。

安全性評估:rentosortib的副作用究竟有多嚴重
有些年頭以前,有份關於肺纖維化的研究報告出現在醫學期刊上,好像是在某個秋天發表的,具體是哪一年其實不太重要,只記得那時候大家對這種病還不是很熟悉。後來又冒出一篇談論nintedanib的文章,說明這藥物治療特發性肺纖維化大概是透過什麼機轉運作,但詳細內容嘛,有人覺得有點複雜,畢竟牽涉到不少生物路徑。
至於pirfenidone呢,最近幾年也有一些討論,不只是針對肺纖維化本身,甚至有人提到可能和心臟衰竭之類的問題略有關聯。CAPACITY計畫那陣子好像做了兩次隨機試驗,大約是在十多年前吧,他們發現pirfenidone在某些病人身上顯示出還算穩定的效果,但並不是所有人都能受益。
nintedanib這個藥也被拿來比一比,那個跨國研究團隊曾經做過調查,涵蓋的人數應該不少,他們關注的不只是療效,也蠻重視安全性的反饋。有趣的是,同一年另外一組學者對pirfenidone進行了三期臨床試驗,看起來結果和前面提到的資料似乎有點呼應但不完全一致。
再往後走,到了這幾年,有關TNIK蛋白質的新角色逐漸浮上檯面,有科學家推測它可能參與癌症、代謝異常或是一些老年疾病的進展——當然這些觀察目前主要還停留在初步階段。AI科技方面,一套名叫PandaOmics的平台慢慢受到重視,它用人工智慧嘗試找尋潛在標靶和生物標誌物,但到底能不能改變現況還需要再觀察。
談到蛋白質和疾病之間錯綜複雜的聯繫,有部分學者靠著多族群的大數據分析和某種遺傳推斷法拼湊出新的圖譜——未來是不是會找到新療法,目前看起來只能說是帶點希望但也不確定。而說到預後,一篇去年的論文列舉了一批跟存活率相關的蛋白質指標,但臨床上真正能派得上用場的大概只有其中少數。
至於最常見的檢查,比如那個大家口中的「強制肺活量」,有人認為它測起來其實挺挑戰信心,每次受檢狀態變動都會讓醫師猶豫要不要信任數字;而另一項氣體擴散能力測試,其實波動幅度也是讓人抓不太準。急性惡化就更難搞了,一旦發生,很可能一下子狀況下滑,有時候醫護團隊只能盡力應對,可惜即使加強觀察,也很難提前預警到底誰會突然惡化。
最後,大約在疫情之前吧,有幾位亞洲地區專家也提出了一些補充意見,不過詳細內容好像沒被廣泛引用,只是偶爾在討論中被帶過而已。
至於pirfenidone呢,最近幾年也有一些討論,不只是針對肺纖維化本身,甚至有人提到可能和心臟衰竭之類的問題略有關聯。CAPACITY計畫那陣子好像做了兩次隨機試驗,大約是在十多年前吧,他們發現pirfenidone在某些病人身上顯示出還算穩定的效果,但並不是所有人都能受益。
nintedanib這個藥也被拿來比一比,那個跨國研究團隊曾經做過調查,涵蓋的人數應該不少,他們關注的不只是療效,也蠻重視安全性的反饋。有趣的是,同一年另外一組學者對pirfenidone進行了三期臨床試驗,看起來結果和前面提到的資料似乎有點呼應但不完全一致。
再往後走,到了這幾年,有關TNIK蛋白質的新角色逐漸浮上檯面,有科學家推測它可能參與癌症、代謝異常或是一些老年疾病的進展——當然這些觀察目前主要還停留在初步階段。AI科技方面,一套名叫PandaOmics的平台慢慢受到重視,它用人工智慧嘗試找尋潛在標靶和生物標誌物,但到底能不能改變現況還需要再觀察。
談到蛋白質和疾病之間錯綜複雜的聯繫,有部分學者靠著多族群的大數據分析和某種遺傳推斷法拼湊出新的圖譜——未來是不是會找到新療法,目前看起來只能說是帶點希望但也不確定。而說到預後,一篇去年的論文列舉了一批跟存活率相關的蛋白質指標,但臨床上真正能派得上用場的大概只有其中少數。
至於最常見的檢查,比如那個大家口中的「強制肺活量」,有人認為它測起來其實挺挑戰信心,每次受檢狀態變動都會讓醫師猶豫要不要信任數字;而另一項氣體擴散能力測試,其實波動幅度也是讓人抓不太準。急性惡化就更難搞了,一旦發生,很可能一下子狀況下滑,有時候醫護團隊只能盡力應對,可惜即使加強觀察,也很難提前預警到底誰會突然惡化。
最後,大約在疫情之前吧,有幾位亞洲地區專家也提出了一些補充意見,不過詳細內容好像沒被廣泛引用,只是偶爾在討論中被帶過而已。

肺功能改善的驚人證據:FVC數據背後的意義
有些人說急性惡化的特發性肺纖維化(IPF)好像並不算罕見,遇到這種情況的大概也有不少患者。Koh跟Kim在那份報告裡提到,出現這種狀況的機率,大致上讓臨床醫師感受到一股棘手氣氛,至於哪些因子會增加風險,好像還沒完全搞清楚,只知道結局大多數時候都不是太理想。Richeldi他們團隊嘗試過一種對磷酸二酯酶4B比較有選擇性的抑制劑,用在IPF身上,看起來或許能帶來一些新方向,但效果如何,還得等後續討論。
病毒感染,Wootton等人倒是做過調查。他們描述,在IPF急性惡化時發現病毒蹤跡的比例,不算極高但也不是少數,那個影響目前看來還需要更多證據去釐清。有一個國際工作小組寫了份報告(Collard主筆),內容細節挺多,把急性惡化的定義、診斷方式以及管理建議分門別類講了一通,只是實際應用起來,每家醫院似乎都有些微差異。
生物標誌物部分倒是變得越來越熱鬧,有如Matrix metalloproteinase-10和LTBP2這類蛋白質,被認為可能跟IPF有關聯。Sokai和Enomoto兩組人在不同時間點談到了它們,一個說MMP-10可能成為新型指標,另一位則覺得LTBP2也是值得關注的潛在訊號。不過,有研究又指出LTBP2在結締組織疾病相關間質性肺病與IPF之間,也許能幫助鑑別,但目前樣本數看起來還偏少。
話題跳一下,其實腎細胞癌領域曾經有人研究蛋白酪氨酸磷酸酶ζ,它會促進β-連環素進入細胞核,提高細胞增殖能力(Shang他們那篇),雖然主題不同,但β-連環素這條路徑在肺纖維化卻也被點名過。Chilosi等人的文章裡提到Wnt/β-catenin訊號異常活躍,而Hu及其同事最近又補充,如果Dec1缺失,好像可以透過PI3K/AKT/GSK-3β/β-catenin這套整合路徑改善肺纖維化現象,但目前僅限於初步觀察。
再往下拉,有些學者開始專注於COL1A1基因調控。Devos小組仔細梳理了這條線上各式調節者名單,可惜資訊量大卻仍未畫下句點;而Bibaki團隊則從miR-185、miR-29a著手,他們發現在IPF與肺癌患者支氣管灌洗液中表現差異有限,不過共同靶向DNMT1和COL1A1時,好像又展現某種病程特異性。Wan和他的夥伴則習慣用生物資訊學工具分析網絡,希望找出那些最重要的基因和通路,但即便如此,目前距離臨床直接應用似乎還早一些。
病毒感染,Wootton等人倒是做過調查。他們描述,在IPF急性惡化時發現病毒蹤跡的比例,不算極高但也不是少數,那個影響目前看來還需要更多證據去釐清。有一個國際工作小組寫了份報告(Collard主筆),內容細節挺多,把急性惡化的定義、診斷方式以及管理建議分門別類講了一通,只是實際應用起來,每家醫院似乎都有些微差異。
生物標誌物部分倒是變得越來越熱鬧,有如Matrix metalloproteinase-10和LTBP2這類蛋白質,被認為可能跟IPF有關聯。Sokai和Enomoto兩組人在不同時間點談到了它們,一個說MMP-10可能成為新型指標,另一位則覺得LTBP2也是值得關注的潛在訊號。不過,有研究又指出LTBP2在結締組織疾病相關間質性肺病與IPF之間,也許能幫助鑑別,但目前樣本數看起來還偏少。
話題跳一下,其實腎細胞癌領域曾經有人研究蛋白酪氨酸磷酸酶ζ,它會促進β-連環素進入細胞核,提高細胞增殖能力(Shang他們那篇),雖然主題不同,但β-連環素這條路徑在肺纖維化卻也被點名過。Chilosi等人的文章裡提到Wnt/β-catenin訊號異常活躍,而Hu及其同事最近又補充,如果Dec1缺失,好像可以透過PI3K/AKT/GSK-3β/β-catenin這套整合路徑改善肺纖維化現象,但目前僅限於初步觀察。
再往下拉,有些學者開始專注於COL1A1基因調控。Devos小組仔細梳理了這條線上各式調節者名單,可惜資訊量大卻仍未畫下句點;而Bibaki團隊則從miR-185、miR-29a著手,他們發現在IPF與肺癌患者支氣管灌洗液中表現差異有限,不過共同靶向DNMT1和COL1A1時,好像又展現某種病程特異性。Wan和他的夥伴則習慣用生物資訊學工具分析網絡,希望找出那些最重要的基因和通路,但即便如此,目前距離臨床直接應用似乎還早一些。
血液蛋白質組學揭示的治療機制與生物標記
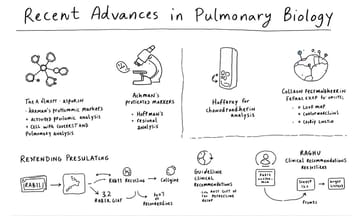
有些人說,在二零二一年那會兒,分子生物科學期刊裡頭曾經有過一篇篇幅不算短的文章,但我記得好像也沒太多人特別在意。倒是後來黃姓研究團隊,好像聚焦在那種叫Asporin的蛋白,他們提出這東西可能對TGF-β誘導的肺部肌成纖維細胞分化有點影響,主要是透過Rab11去幫忙TβRI的回收,不過詳細流程聽起來還挺複雜。他們發表在美國呼吸與細胞分子生物學雜誌上,大概是在去年左右吧。
另一批瑞典的Åhrman等人,早些時候搞了個定量蛋白質體分析,專門鑽研慢性阻塞性肺病還有特發性肺纖維化患者的肺外基質組成。說真的,那份資料量感覺蠻龐大的,我印象中分析方法也頗為細緻。不過再往前翻,大約十多年前,Acharya他們對於所謂活化型纖維母細胞蛋白也下了點功夫——這類酶跟肺部重塑界面關係密切,只是具體作用機轉說法其實還不少。
至於新近一兩年,美國那邊Hoffman帶著人做了區域性的肺外基質分析,比較不同疾病狀態下的人類樣本,看來內容相當細膩;但究竟這些差異是不是真的能直接反映臨床情形,我覺得還需要後續觀察。
如果要談和骨骼相關的黏附蛋白,有個Shum寫過Chondroadherin如何跟第二型膠原結合,其實資料並不多,可惜後來討論度沒很高。然後Raghu領銜制定的肺纖維化臨床指引,到現在都還有人拿出來當參考依據,他們給出的建議通常比較中庸,不容易看到什麼太偏激的用語。
技術層面呢,美加歐洲協會聯手更新過一次肺功能測試標準(大約四五年前),比如單次吸入一氧化碳檢查法那些,都強調流程一致性。我記得Graham這名字出現了不只一次,也許是因為他參與訂標準文件挺久了。
講到咳嗽評估工具,那個李斯特咳嗽問卷(LCQ)一直被提起,好像從將近二十年前開始流行。有篇文獻曾討論它在慢阻肺及長期咳嗽族群裡頭精確度如何;而針對咳痰或自覺症狀變化,有些研究則指出,只要改變幅度達到某個大家普遍接受的數值範圍,患者通常會自己察覺得到改善。不過每家醫院收案條件不太一樣,所以數據多少都有點浮動。
另一批瑞典的Åhrman等人,早些時候搞了個定量蛋白質體分析,專門鑽研慢性阻塞性肺病還有特發性肺纖維化患者的肺外基質組成。說真的,那份資料量感覺蠻龐大的,我印象中分析方法也頗為細緻。不過再往前翻,大約十多年前,Acharya他們對於所謂活化型纖維母細胞蛋白也下了點功夫——這類酶跟肺部重塑界面關係密切,只是具體作用機轉說法其實還不少。
至於新近一兩年,美國那邊Hoffman帶著人做了區域性的肺外基質分析,比較不同疾病狀態下的人類樣本,看來內容相當細膩;但究竟這些差異是不是真的能直接反映臨床情形,我覺得還需要後續觀察。
如果要談和骨骼相關的黏附蛋白,有個Shum寫過Chondroadherin如何跟第二型膠原結合,其實資料並不多,可惜後來討論度沒很高。然後Raghu領銜制定的肺纖維化臨床指引,到現在都還有人拿出來當參考依據,他們給出的建議通常比較中庸,不容易看到什麼太偏激的用語。
技術層面呢,美加歐洲協會聯手更新過一次肺功能測試標準(大約四五年前),比如單次吸入一氧化碳檢查法那些,都強調流程一致性。我記得Graham這名字出現了不只一次,也許是因為他參與訂標準文件挺久了。
講到咳嗽評估工具,那個李斯特咳嗽問卷(LCQ)一直被提起,好像從將近二十年前開始流行。有篇文獻曾討論它在慢阻肺及長期咳嗽族群裡頭精確度如何;而針對咳痰或自覺症狀變化,有些研究則指出,只要改變幅度達到某個大家普遍接受的數值範圍,患者通常會自己察覺得到改善。不過每家醫院收案條件不太一樣,所以數據多少都有點浮動。
為什麼60mg劑量組展現出最顯著的療效
如果要說這些參考文獻,裡頭好像有幾篇是跟呼吸道疾病量表驗證有關的,像那個Leicester咳嗽問卷,不只是針對囊腫性纖維化以外的支氣管擴張症,好像也延伸到慢性咳嗽患者。不過具體數據都是用一些將近一半或者七十多位病人來做統計,沒有精確到每一個細節。然後你還會看到今年初出的Reactome Pathway Knowledgebase,主要談生物資料庫,但和臨床直接關聯倒也不太明顯。
感謝名單就比較長了,有一大堆組織跟公司參與,像英國利茲那邊的Fortrea Clinical Pharmacology Services,大概負責協調和現場安排;然後上海Insilico Medicine的一些成員,好像有人專門處理資料,也有人在臨床操作上給協助,美國麻省那邊還有人幫忙看結果。這些人分布很廣,美國、中國、阿聯酋、香港都有蹤影,看起來跨國合作還蠻明顯,只是具體誰主導哪塊其實不完全清楚。
作者相關資訊寫得細碎,基本上就是各大醫院的呼吸重症部門和Insilico團隊的人混合組成,北京、天津、西南、華中甚至海南都有醫師參與。人名很多,記得下來有點困難。有意思的是,有些人的名字在不同地區Insilico團隊都出現,比如Alex Zhavoronkov,他同時掛了美國、阿布達比和香港三地的身份,看起來應該算是主要推手之一吧。
至於大家各自做了什麼,好像也不是劃分得特別明確。有幾位比較偏向設計和發想臨床試驗,大約由五六個核心人物領頭;執行面則是好幾家醫院輪流負責招募病患及收集數據,人數可能將近二十位上下。分析資料這段,除了中國內地的技術團隊,好像美國那邊也有加入一起討論和解讀。不過中間細節應該還有沒被記載的小插曲或調整。
總之,就是一種多方協作但分工稍嫌模糊的大型臨床研究模式,各自貢獻了一部分力量,有些角色可能重疊,也不排除誰在某階段出力特別多,但很難從表面文字就斷定權重如何。
感謝名單就比較長了,有一大堆組織跟公司參與,像英國利茲那邊的Fortrea Clinical Pharmacology Services,大概負責協調和現場安排;然後上海Insilico Medicine的一些成員,好像有人專門處理資料,也有人在臨床操作上給協助,美國麻省那邊還有人幫忙看結果。這些人分布很廣,美國、中國、阿聯酋、香港都有蹤影,看起來跨國合作還蠻明顯,只是具體誰主導哪塊其實不完全清楚。
作者相關資訊寫得細碎,基本上就是各大醫院的呼吸重症部門和Insilico團隊的人混合組成,北京、天津、西南、華中甚至海南都有醫師參與。人名很多,記得下來有點困難。有意思的是,有些人的名字在不同地區Insilico團隊都出現,比如Alex Zhavoronkov,他同時掛了美國、阿布達比和香港三地的身份,看起來應該算是主要推手之一吧。
至於大家各自做了什麼,好像也不是劃分得特別明確。有幾位比較偏向設計和發想臨床試驗,大約由五六個核心人物領頭;執行面則是好幾家醫院輪流負責招募病患及收集數據,人數可能將近二十位上下。分析資料這段,除了中國內地的技術團隊,好像美國那邊也有加入一起討論和解讀。不過中間細節應該還有沒被記載的小插曲或調整。
總之,就是一種多方協作但分工稍嫌模糊的大型臨床研究模式,各自貢獻了一部分力量,有些角色可能重疊,也不排除誰在某階段出力特別多,但很難從表面文字就斷定權重如何。
未來展望:AI藥物開發將如何改變醫療產業格局
關於這篇論文的寫作和修訂,A.Z. 也有參與其中。所有作者差不多都在投稿前確認並同意了內容。有些聯繫事宜似乎由徐作軍或Alex Zhavoronkov負責。說到利益揭露,像是F.R.、S.R.、C.S.、S.L.、Y.L.、H.Z.等十來位研究人員,好像都是Insilico Medicine的員工,而這家公司就是贊助這次實驗的單位。其餘作者則沒什麼利益衝突要提。
審查過程倒是有點意思,《Nature Medicine》感謝了Yuben Moodley、Luca Richeldi、Jeff Swigris以及另外幾位沒有公開姓名的審稿人,他們對文章做了一些意見回饋。初步看起來,主要編輯好像是Lorenzo Righetto,不過他們團隊協作也挺密切。
出版方Springer Nature一直強調自己對地圖標示還有機構隸屬關係持中立態度——每次正式發表都會提醒一下讀者。
附錄裡列出的數據還蠻多,有些細節需要慢慢消化。例如那個所謂「延伸數據圖一」,主要畫出試驗標準和隨機分組情況,以及整個治療流程安排。參加研究的人被分成大約四種治療手法:三種不同劑量和頻率的rentosertib(有每天一次或兩次)、再加上一組安慰劑。他們服藥長達將近三個月,每隔一段時間就會抽血檢查或評估肺功能。至於縮寫嘛,像IPF指的是特發性肺纖維化,FVC大概就是強制用力肺活量,FEV1應該跟呼氣能力有關;其他諸如DLCO講的是肺部換氣效率之類——醫院常見縮寫,不太容易記住所有細節。
再往下看,「延伸數據圖二」討論rentosertib治療後十二週時FVC變化。有兩名病患因為篩查階段跟基線測量落差超出六百毫升,被排除在外,其餘人的資料用來計算平均變化值和信賴區間。不過具體多少升多少毫升其實都沒明講,大致上就是比較前後差距,用了帶誤差範圍的方法。如果遇到資料缺失,好像還採用了所謂「多重插補」統計方式處理,看不懂公式也無妨,就是想辦法讓結果更可靠。
接著又聊到如果病患本身還同時用現行抗纖維化藥物(SOC),那麼rentosertib帶來的效果會不會不同。他們把這群人拆開分析,比較沒吃抗纖維化藥和有吃的人,各自的FVC改變情形,也都是用信賴區間描述結果。不過到底哪一組優勢明顯,也沒直接說死,只能看到趨勢。
「延伸數據圖四」則把注意力轉到其他肺部功能指標,比如DLCO(換氣能力)、FEV1(短時間內呼氣量)、甚至連咳嗽問卷分數(LCQ)和六分鐘步行距離都有測試。各項指標呈現出一些起伏,但每個數值背後都伴隨標準差或者誤差,不免讓人覺得真實影響可能還得進一步探究。
到了第五張附表,他們很認真地測試了rentosertib在體內藥物濃度變動,包括給藥初期及十二週後的一些藥動學參數,比如面積曲線AUC0-t或半衰期t1/2等等。患者人數大致上每組十來位左右,有點小規模但能看出趨勢。此外,還探討了藥物濃度跟FVC改變之間可能存在某種相關性,用的是斯皮爾曼相關係數,但結論傾向保留空間——只能說部分患者在某些狀況下似乎有效果。
再往下,「延伸數據圖六」講的是血清蛋白質表現隨時間與劑量改變而產生波動。他們利用了一套線性迴歸模式評估蛋白質濃度上下起伏,再用BH校正方法控制假陽性率。有一些蛋白質特別被黃色框框標註,好像跟纖維化病程比較相關,但是哪些最重要其實也沒完全明朗。同樣地,第七張圖聚焦於那些蛋白表現與肺功能改善之間潛在聯繫,有借助PandaOmics工具交叉比對既往RNA-seq資料集,把健康者跟IPF患者做比較,但只有少部分基因型的蛋白濃度真的展現出顯著相關,而且受訪樣本也是四十多人而已,每組大概十多人不到二十,所以結論僅供參考吧。
第八張補充資料又拉回年齡相關蛋白,例如IL10、CD5還有COL6A3——這幾個名字常常出現在免疫調節或細胞外基質重塑領域。他們嘗試找尋這些蛋白濃度與肺功能改善是否搭得上邊,一邊用皮爾森相關、一邊又套配對t檢定。不管怎麼算,樣本規模有限,所以只能說觀察到某種趨勢,但真要推翻或肯定原理恐怕還早。
最後談授權條款方面,這份文章採取相當開放但又有限制的授權方式:大家可以在非商業情境下分享原文,不過不能擅自改編內容去發佈。如果圖片什麼的不屬於創作者自己,那還得另外詢問版權方才行。有興趣翻閱全文或瞭解授權細節,可以去Creative Commons官網看看條款內容。如果有人想引用文章,官方建議按照Xu等人的格式註明來源就好。而且整份研究從二零二四年底送件,到隔年春天才被接受,大約花了半年多才公開發表。不過具體哪一天刊登,其實不是大家都記得很清楚,就六月初左右吧。
審查過程倒是有點意思,《Nature Medicine》感謝了Yuben Moodley、Luca Richeldi、Jeff Swigris以及另外幾位沒有公開姓名的審稿人,他們對文章做了一些意見回饋。初步看起來,主要編輯好像是Lorenzo Righetto,不過他們團隊協作也挺密切。
出版方Springer Nature一直強調自己對地圖標示還有機構隸屬關係持中立態度——每次正式發表都會提醒一下讀者。
附錄裡列出的數據還蠻多,有些細節需要慢慢消化。例如那個所謂「延伸數據圖一」,主要畫出試驗標準和隨機分組情況,以及整個治療流程安排。參加研究的人被分成大約四種治療手法:三種不同劑量和頻率的rentosertib(有每天一次或兩次)、再加上一組安慰劑。他們服藥長達將近三個月,每隔一段時間就會抽血檢查或評估肺功能。至於縮寫嘛,像IPF指的是特發性肺纖維化,FVC大概就是強制用力肺活量,FEV1應該跟呼氣能力有關;其他諸如DLCO講的是肺部換氣效率之類——醫院常見縮寫,不太容易記住所有細節。
再往下看,「延伸數據圖二」討論rentosertib治療後十二週時FVC變化。有兩名病患因為篩查階段跟基線測量落差超出六百毫升,被排除在外,其餘人的資料用來計算平均變化值和信賴區間。不過具體多少升多少毫升其實都沒明講,大致上就是比較前後差距,用了帶誤差範圍的方法。如果遇到資料缺失,好像還採用了所謂「多重插補」統計方式處理,看不懂公式也無妨,就是想辦法讓結果更可靠。
接著又聊到如果病患本身還同時用現行抗纖維化藥物(SOC),那麼rentosertib帶來的效果會不會不同。他們把這群人拆開分析,比較沒吃抗纖維化藥和有吃的人,各自的FVC改變情形,也都是用信賴區間描述結果。不過到底哪一組優勢明顯,也沒直接說死,只能看到趨勢。
「延伸數據圖四」則把注意力轉到其他肺部功能指標,比如DLCO(換氣能力)、FEV1(短時間內呼氣量)、甚至連咳嗽問卷分數(LCQ)和六分鐘步行距離都有測試。各項指標呈現出一些起伏,但每個數值背後都伴隨標準差或者誤差,不免讓人覺得真實影響可能還得進一步探究。
到了第五張附表,他們很認真地測試了rentosertib在體內藥物濃度變動,包括給藥初期及十二週後的一些藥動學參數,比如面積曲線AUC0-t或半衰期t1/2等等。患者人數大致上每組十來位左右,有點小規模但能看出趨勢。此外,還探討了藥物濃度跟FVC改變之間可能存在某種相關性,用的是斯皮爾曼相關係數,但結論傾向保留空間——只能說部分患者在某些狀況下似乎有效果。
再往下,「延伸數據圖六」講的是血清蛋白質表現隨時間與劑量改變而產生波動。他們利用了一套線性迴歸模式評估蛋白質濃度上下起伏,再用BH校正方法控制假陽性率。有一些蛋白質特別被黃色框框標註,好像跟纖維化病程比較相關,但是哪些最重要其實也沒完全明朗。同樣地,第七張圖聚焦於那些蛋白表現與肺功能改善之間潛在聯繫,有借助PandaOmics工具交叉比對既往RNA-seq資料集,把健康者跟IPF患者做比較,但只有少部分基因型的蛋白濃度真的展現出顯著相關,而且受訪樣本也是四十多人而已,每組大概十多人不到二十,所以結論僅供參考吧。
第八張補充資料又拉回年齡相關蛋白,例如IL10、CD5還有COL6A3——這幾個名字常常出現在免疫調節或細胞外基質重塑領域。他們嘗試找尋這些蛋白濃度與肺功能改善是否搭得上邊,一邊用皮爾森相關、一邊又套配對t檢定。不管怎麼算,樣本規模有限,所以只能說觀察到某種趨勢,但真要推翻或肯定原理恐怕還早。
最後談授權條款方面,這份文章採取相當開放但又有限制的授權方式:大家可以在非商業情境下分享原文,不過不能擅自改編內容去發佈。如果圖片什麼的不屬於創作者自己,那還得另外詢問版權方才行。有興趣翻閱全文或瞭解授權細節,可以去Creative Commons官網看看條款內容。如果有人想引用文章,官方建議按照Xu等人的格式註明來源就好。而且整份研究從二零二四年底送件,到隔年春天才被接受,大約花了半年多才公開發表。不過具體哪一天刊登,其實不是大家都記得很清楚,就六月初左右吧。




